2019年7月11日,张锋等人在Science 在线发表题为“A cytosine deaminase for programmable single-base RNA editing”的研究论文,该研究通过定向蛋白进化将ADAR2转化为胞苷脱氨酶,称为特定C到U交换的RNA编辑(RESCUE)。 RESCUE使RNA编辑可靶向的致病突变数量增加一倍,并能够调节磷酸化信号相关残基。 研究人员应用RESCUE来驱动β-catenin激活和细胞生长。 此外,RESCUE保留A到I的编辑活性,通过使用定制的指导RNA实现多重C到U和A到I的编辑。RESCUE是一种可编程的碱基编辑工具,能够在RNA中精确地进行胞苷至尿苷的转换。 总体而言,RESCUE通过新的基础编辑功能扩展了RNA靶向工具包,允许扩展建模和遗传疾病的潜在治疗。
2019年6月20日,美国博德研究所张锋等人在Cell 发表题为”DNA Microscopy: Optics-free Spatio-genetic Imaging by a Stand-Alone Chemical Reaction“的研究论文,该研究展示了DNA显微镜,这是一种独特的成像模式,可用于相对生物分子位置的可扩展,无光学映射。在转录物的DNA显微镜检查中,转录物分子用随机核苷酸原位标记,特异的标记每个分子。第二次原位反应然后扩增标记的分子,连接所得的拷贝,并添加新的随机化核苷酸以唯一地标记每个连锁事件。算法解码来自这些连锁序列的分子邻近性,并以精确的序列信息推断细胞分辨率的原始转录物的物理图像。由于其成像能力完全来自扩散分子动力学,因此DNA显微镜构成化学编码的显微镜系统;
2019年6月6日,美国博德研究所张锋在Science 在线发表题为“RNA-guided DNA insertion with CRISPR-associated transposases”的研究论文,该研究表征来自蓝细菌Scytonema hofmanni的CRISPR相关转座酶(CAST),其由Tn7样转座酶亚基和V-K CRISPR效应物(Cas12k)组成。ShCAST通过在原型间隔区下游60-66bp处定向插入DNA片段,该过程是催化RNA指导的DNA转座。ShCAST将DNA整合到大肠杆菌基因组中的独特位点,频率高达80%,无需正选择。 这项工作扩展了对CRISPR-Cas系统功能多样性的理解,并建立了精确DNA插入的范例。

先前张锋等人开发了一种名为REPAIR的RNA碱基编辑技术(用于可编程A到I(G)置换的RNA编辑),通过将催化灭活的RNA靶向CRISPR-Cas13(dCas13)与ADAR2的腺嘌呤脱氨酶结构域融合,开发出可A至I RNA编辑方法。

张锋
然而,REPAIR以及许多其他RNA编辑技术仅允许A到I的转换。用于精确RNA编辑胞苷至尿苷的技术将极大地扩展疾病突变和蛋白质修饰的范围。
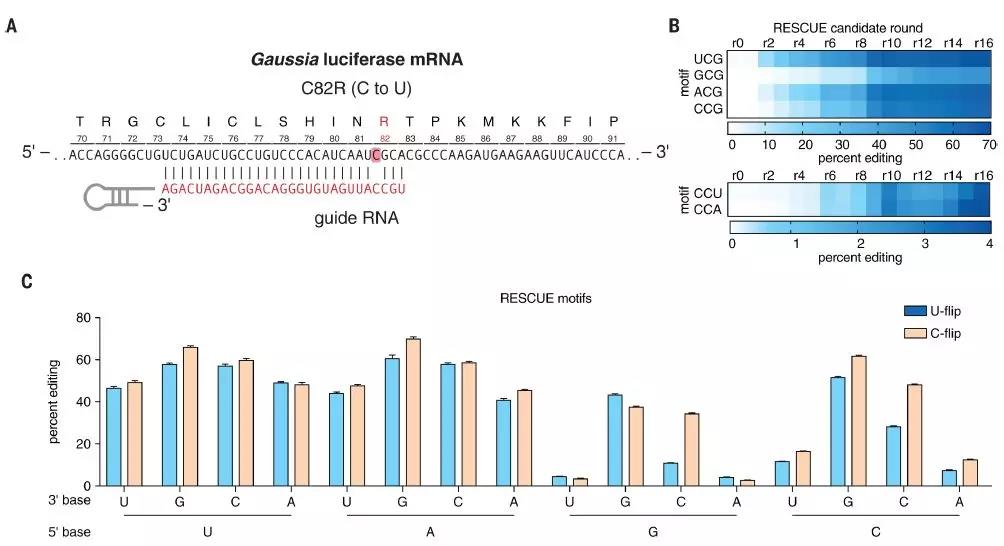
用于胞苷脱氨基的ADAR2脱氨酶结构域的进
尽管已经利用能够催化C至U转化的天然酶进行DNA碱基编辑,但它们仅在单链底物上运行,表现出脱靶,并且在多个碱基内脱氨基。在这里,研究人员通过直接将ADAR2转化为胞苷脱氨酶,称为特定C到U交换的RNA编辑(RESCUE)。
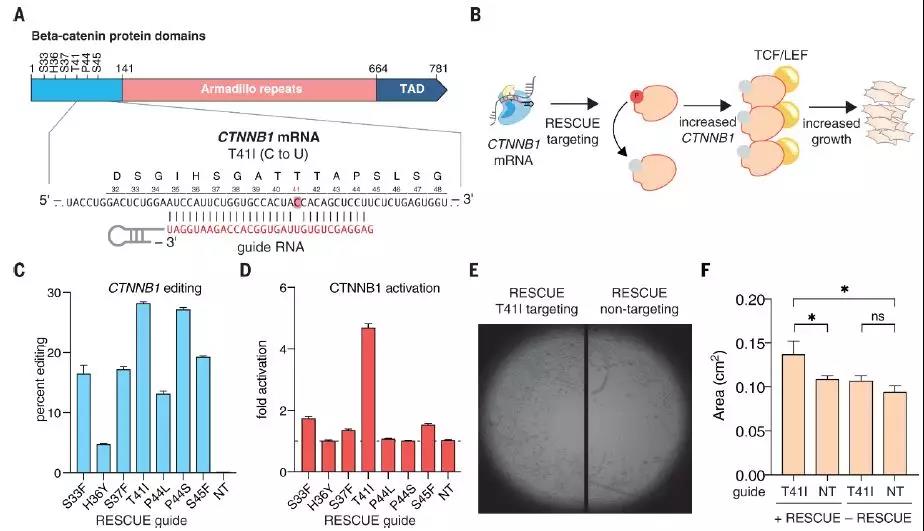
RESCUE对细胞生长和信号传导的表型结果
RESCUE使RNA编辑可靶向的致病突变数量增加一倍,并能够调节磷酸化信号相关残基。 研究人员应用RESCUE来驱动β-catenin激活和细胞生长。此外,RESCUE保留A到I的编辑活性,通过使用定制的指导RNA实现多重C到U和A到I的编辑。
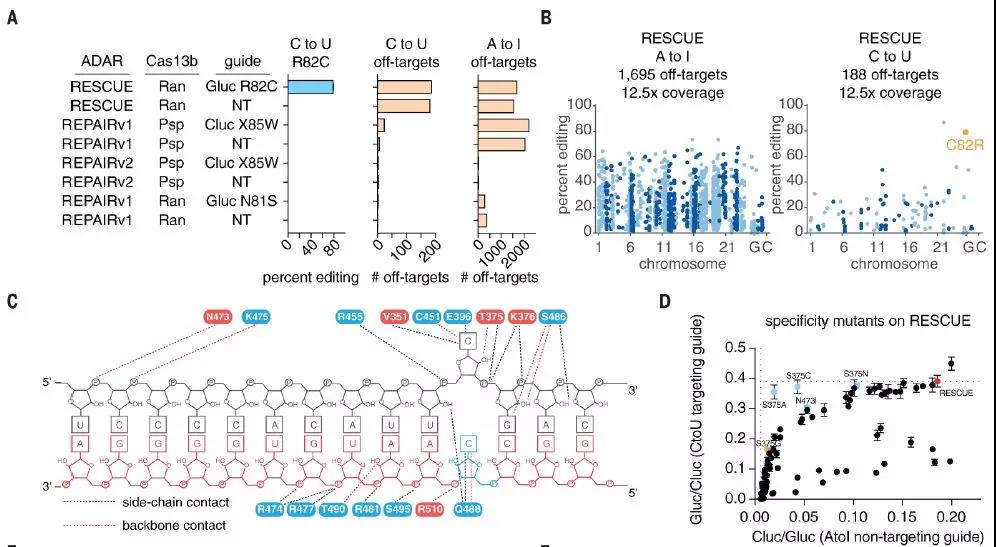
转录组范围内的RESCUE特异性
RESCUE是一种可编程的碱基编辑工具,能够在RNA中精确地进行胞苷至尿苷的转换。 总体而言,RESCUE通过新的基础编辑功能扩展了RNA靶向工具包,允许扩展建模和遗传疾病的潜在治疗。





